–°—А–Њ—З–љ–∞—П –њ—Г–±–ї–Є–Ї–∞—Ж–Є—П –љ–∞—Г—З–љ–Њ–є —Б—В–∞—В—М–Є
+7 995 770 98 40
+7 995 202 54 42
info@journalpro.ru
–Р–љ—В–Є–Ї–Њ—А—А–Њ–Ј–Є–є–љ—Л–є —Н—Д—Д–µ–Ї—В –ґ–µ–ї–µ–Ј–љ–Њ–≥–Њ —Б—В–Њ–ї–±–∞ –Ъ—Г—В—Г–±-–Ь–Є–љ–∞—А –і–µ–Љ–Њ–љ—Б—В—А–Є—А—Г–µ—В —Г—З–µ–±–љ–Њ вАУ –љ–∞–≥–ї—П–і–љ–Њ–µ –њ–Њ—Б–Њ–±–Є–µ.
–†—Г–±—А–Є–Ї–∞: –Ґ–µ—Е–љ–Є—З–µ—Б–Ї–Є–µ –љ–∞—Г–Ї–Є
–Ц—Г—А–љ–∞–ї: «–Х–≤—А–∞–Ј–Є–є—Б–Ї–Є–є –Э–∞—Г—З–љ—Л–є –Ц—Г—А–љ–∞–ї вДЦ12 2015» (–і–µ–Ї–∞–±—А—М 2015)
–Ъ–Њ–ї–Є—З–µ—Б—В–≤–Њ –њ—А–Њ—Б–Љ–Њ—В—А–Њ–≤ —Б—В–∞—В—М–Є: 4071
–Я–Њ–Ї–∞–Ј–∞—В—М PDF –≤–µ—А—Б–Є—О –Р–љ—В–Є–Ї–Њ—А—А–Њ–Ј–Є–є–љ—Л–є —Н—Д—Д–µ–Ї—В –ґ–µ–ї–µ–Ј–љ–Њ–≥–Њ —Б—В–Њ–ї–±–∞ –Ъ—Г—В—Г–±-–Ь–Є–љ–∞—А –і–µ–Љ–Њ–љ—Б—В—А–Є—А—Г–µ—В —Г—З–µ–±–љ–Њ вАУ –љ–∞–≥–ї—П–і–љ–Њ–µ –њ–Њ—Б–Њ–±–Є–µ.
–Ч–Њ–ї–Њ—В–Њ–≤–∞ –Ґ–∞—В—М—П–љ–∞ –°—В–∞–љ–Є—Б–ї–∞–≤–Њ–≤–љ–∞ / Zolotova Tatiana Stanislavovna вАУ –Ф–Є—А–µ–Ї—В–Њ—А –С–Є–Ј–љ–µ—Б –Х–і–Є–љ–Є—Ж—Л –Ю–Ю–Ю "–Р. –Т. –Х.", –≥. –Ь–Њ—Б–Ї–≤–∞,
–Ъ–ї–Є–Љ–µ–љ–Ї–Њ –Ю–ї—М–≥–∞ –С–Њ—А–Є—Б–Њ–≤–љ–∞ / Klimenko Olga Borisovna вАУ –≤–µ–і—Г—Й–Є–є –Є–љ–ґ–µ–љ–µ—А, –Я–Р–Ю –Ъ–Ь–Ч, –≥. –Ъ—А–∞—Б–љ–Њ–≥–Њ—А—Б–Ї,
–†–µ–≤–∞—И–Є–љ –С–Њ—А–Є—Б –У–µ–љ–љ–∞–і—М–µ–≤–Є—З / Revashin Boris Genadievich вАУ –Є–љ–ґ–µ–љ–µ—А, –Я–Р–Ю –Ъ–Ь–Ч, –≥. –Ъ—А–∞—Б–љ–Њ–≥–Њ—А—Б–Ї.
–Ъ–ї—О—З–µ–≤—Л–µ —Б–ї–Њ–≤–∞: –∞–љ—В–Є–Ї–Њ—А—А–Њ–Ј–Є–є–љ—Л–є —Н—Д—Д–µ–Ї—В; –ґ–µ–ї–µ–Ј–љ—Л–є —Б—В–Њ–ї–± –Љ–Є–љ–∞—А–µ—В–∞ –Ъ—Г—В—Г–±-–Ь–Є–љ–∞—А; —Г—З–µ–±–љ–Њ вАУ –љ–∞–≥–ї—П–і–љ–Њ–µ –њ–Њ—Б–Њ–±–Є–µ.
–£—З–µ–±–љ–Њ вАУ –љ–∞–≥–ї—П–і–љ–Њ–µ –њ–Њ—Б–Њ–±–Є–µ –і–ї—П –і–µ–Љ–Њ–љ—Б—В—А–∞—Ж–Є–Є —Н—Д—Д–µ–Ї—В–∞ –∞–љ—В–Є–Ї–Њ—А—А–Њ–Ј–Є–Њ–љ–љ–Њ–є —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є –ґ–µ–ї–µ–Ј–љ–Њ–≥–Њ —Б—В–Њ–ї–±–∞ –Љ–Є–љ–∞—А–µ—В–∞ –Ъ—Г—В—Г–± вАУ –Ь–Є–љ–∞—А –Љ–Њ–ґ–µ—В –њ—А–Є–Љ–µ–љ—П—В—М—Б—П –≤ —Г—З—А–µ–ґ–і–µ–љ–Є—П—Е –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П, –≤—Л–њ–Њ–ї–љ—П—О—Й–Є—Е –њ–Њ–і–≥–Њ—В–Њ–≤–Ї—Г —Б–њ–µ—Ж–Є–∞–ї–Є—Б—В–Њ–≤ —Б –њ—А–µ–њ–Њ–і–∞–≤–∞–љ–Є–µ–Љ –і–Є—Б—Ж–Є–њ–ї–Є–љ: —Е–Є–Љ–Є—П; –љ–µ–Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–∞—П —Е–Є–Љ–Є—П; —Н–ї–µ–Ї—В—А–Њ—Е–Є–Љ–Є—П; –Љ–µ—В–∞–ї–ї–Њ–≤–µ–і–µ–љ–Є–µ; —В–µ–Њ—А–Є—П –Ї–Њ—А—А–Њ–Ј–Є–Є; —Д–Є–Ј–Є–Ї–∞ —В–≤—С—А–і–Њ–≥–Њ —В–µ–ї–∞; –Ї–≤–∞–љ—В–Њ–≤–∞—П —Д–Є–Ј–Є–Ї–∞.
–Т–∞—А–Є–∞–љ—В—Л –Ї–Њ–Љ–њ–ї–µ–Ї—В–Њ–≤ –њ–Њ—Б–Њ–±–Є–є —Б–Њ–і–µ—А–ґ–∞—В: –Љ–µ—В–Њ–і–Є—З–µ—Б–Ї–Є–µ –Љ–∞—В–µ—А–Є–∞–ї—Л; –Њ–њ–Є—Б–∞–љ–Є–µ —Б—Г—Й–љ–Њ—Б—В–Є –љ–∞—Г—З–љ–Њ–≥–Њ –Њ—В–Ї—А—Л—В–Є—П [–Ы1]; –ї–µ–Ї—Ж–Є–Њ–љ–љ—Л–µ –Љ–∞—В–µ—А–Є–∞–ї—Л —Б –Є–ї–ї—О—Б—В—А–∞—Ж–Є—П–Љ–Є; —В–µ—Е–љ–Є—З–µ—Б–Ї–Є–µ —Б—А–µ–і—Б—В–≤–∞ –і–µ–Љ–Њ–љ—Б—В—А–∞—Ж–Є–Є –Є –љ–∞–±–ї—О–і–µ–љ–Є—П —Н—Д—Д–µ–Ї—В–∞ –Є –Є–љ—Б—В—А—Г–Ї—Ж–Є–Є –њ–Њ –Є—Е –њ—А–Є–Љ–µ–љ–µ–љ–Є—О; –њ–ї–∞–љ—Л –њ—А–Њ–≤–µ–і–µ–љ–Є—П –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л—Е —А–∞–±–Њ—В; –Њ–і–Є–љ–∞–Ї–Њ–≤—Л–µ –ґ–µ–ї–µ–Ј–љ—Л–µ –њ–ї–∞—Б—В–Є–љ—Л –і–ї–Є–љ–Њ–є 30 –Љ–Љ., —И–Є—А–Є–љ–Њ–є 10 –Љ–Љ., —В–Њ–ї—Й–Є–љ–Њ–є 1 –Љ–Љ. –Т –љ–∞—З–∞–ї–µ –Њ–њ—Л—В–∞ –њ—А–Њ–Є–Ј–≤–Њ–ї—М–љ–Њ –≤—Л–±–Є—А–∞—О—В—Б—П –Ї–Њ–љ—В—А–Њ–ї—М–љ–∞—П –њ–ї–∞—Б—В–Є–љ–∞ –Є –Є—Б–њ—Л—В—Г–µ–Љ–∞—П –њ–ї–∞—Б—В–Є–љ–∞ –Є –љ–∞ –Є—Е –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –љ–∞–љ–Њ—Б—П—В—Б—П –Ї–∞–њ–ї–Є –≤–Њ–і—Л.
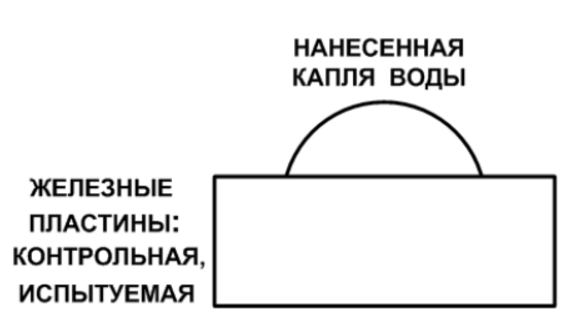
–Т—Л—Б—Л—Е–∞–љ–Є–µ –Ї–∞–њ–µ–ї—М –≤–Њ–і—Л –љ–∞ –њ–ї–∞—Б—В–Є–љ–∞—Е –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –Ј–∞ 45 вАУ 55 –Љ–Є–љ—Г—В –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л –Є –≤–ї–∞–ґ–љ–Њ—Б—В–Є –Њ–Ї—А—Г–ґ–∞—О—Й–µ–≥–Њ –≤–Њ–Ј–і—Г—Е–∞.
–§–∞–Ј—Л –њ—А–Є –≤—Л—Б—Л—Е–∞–љ–Є–Є –Њ—В–і–µ–ї—М–љ–Њ–є –Ї–∞–њ–ї–Є –≤–Њ–і—Л –љ–∞ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –ґ–µ–ї–µ–Ј–љ–Њ–є –њ–ї–∞—Б—В–Є–љ–µ: –њ–µ—А–≤—Л–µ 5 вАУ 12 –Љ–Є–љ—Г—В –љ–∞–±–ї—О–і–∞–µ—В—Б—П —Д–∞–Ј–∞ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –≥–Є–і—А–Њ–Ї—Б–Є–і–∞ –ґ–µ–ї–µ–Ј–∞ Fe(OH)2. –≠—В–Њ –љ–µ—Г—Б—В–Њ–є—З–Є–≤–Њ–µ —Б–Њ–µ–і–Є–љ–µ–љ–Є–µ —Б–µ—А–Њ–≥–Њ –Є–ї–Є —Б–≤–µ—В–ї–Њ вАУ —Б–µ—А–Њ–≥–Њ —Ж–≤–µ—В–∞, –њ–ї–Њ—Е–Њ —А–∞—Б—В–≤–Њ—А–Є–Љ–Њ–µ –≤ –≤–Њ–і–µ, –љ–µ –љ–∞—А—Г—И–∞–µ—В –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ—Г—О —Б—В—А—Г–Ї—В—Г—А—Г –ґ–µ–ї–µ–Ј–∞.
![]()
–≠–ї–µ–Ї—В—А–Њ–љ—Л –≤—Л—Е–Њ–і—П—В —Б –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –ґ–µ–ї–µ–Ј–∞ –≤ –Ї–∞–њ–ї—О –≤–Њ–і—Л. –Ч–∞—В–µ–Љ –љ–∞—З–Є–љ–∞–µ—В—Б—П —Д–∞–Ј–∞ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П —А–ґ–∞–≤—З–Є–љ—Л:
![]()
–≠—В–Њ —Г—Б—В–Њ–є—З–Є–≤–Њ–µ, –љ–µ—А–∞—Б—В–≤–Њ—А–Є–Љ–Њ–µ –≤ –≤–Њ–і–µ —Е–Є–Љ–Є—З–µ—Б–Ї–Њ–µ —Б–Њ–µ–і–Є–љ–µ–љ–Є–µ –Ї–Њ—А–Є—З–љ–µ–≤–Њ–≥–Њ –Є–ї–Є –Ї—А–∞—Б–љ–Њ вАУ –Ї–Њ—А–Є—З–љ–µ–≤–Њ–≥–Њ —Ж–≤–µ—В–∞, –Њ–љ–Њ –љ–µ–Њ–±—А–∞—В–Є–Љ–Њ –Є–Ј–Љ–µ–љ—П–µ—В –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ—Г—О —Б—В—А—Г–Ї—В—Г—А—Г –ґ–µ–ї–µ–Ј–∞ [–Ы2 —Б—В—А. 623 вАУ 625, –Ы3 —Б—В—А. 130]. –Э–∞ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –њ–ї–∞—Б—В–Є–љ—Л –њ–Њ–і –Ї–∞–њ–ї–µ–є –≤–Њ–і—Л –Њ–±—А–∞–Ј—Г—О—В—Б—П –∞–љ–Њ–і–љ—Л–µ —Г—З–∞—Б—В–Ї–Є
![]()
–Є –Ї–∞—В–Њ–і–љ—Л–µ —Г—З–∞—Б—В–Ї–Є
![]()
–†–Є—Б—Г–љ–Њ–Ї 2 вАУ –Ї–Њ–њ–Є—П –†–Є—Б. 18.8 —Б–Њ —Б—В—А. 624, [–Ы2] –њ–Њ–ї–љ–Њ –Є –љ–∞–≥–ї—П–і–љ–Њ –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б—Е–µ–Љ—Г –њ—А–Њ—Ж–µ—Б—Б–∞ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П —А–ґ–∞–≤—З–Є–љ—Л.
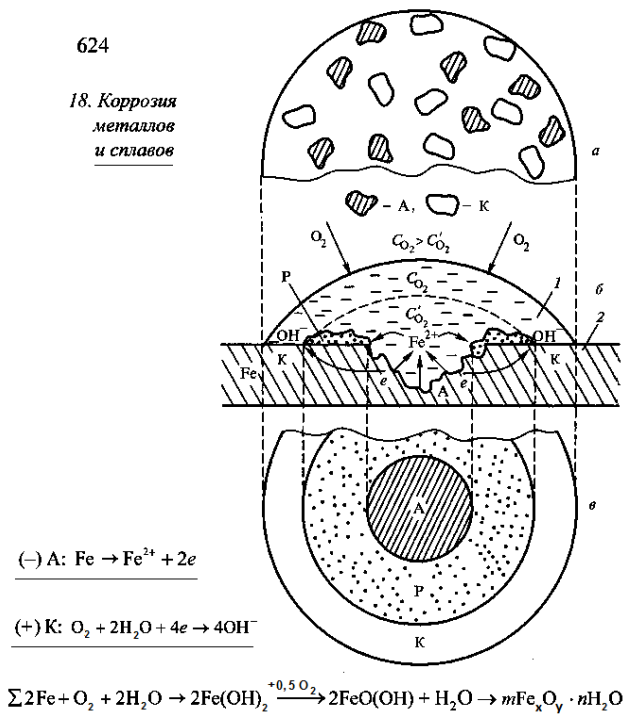
–Э–∞ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –њ–ї–∞—Б—В–Є–љ–µ –љ–∞—А—Г—И–∞—О—В—Б—П —Н–Ї–≤–Є–њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ–Њ—Б—В—М –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –ґ–µ–ї–µ–Ј–∞ –Є —Н–ї–µ–Ї—В—А–Њ–љ–љ–Њ вАУ –Є–Њ–љ–љ—Л–є –±–∞–ї–∞–љ—Б –≤ –Ї—А–Є—Б—В–∞–ї–ї–Є—З–µ—Б–Ї–Њ–є —А–µ—И—С—В–Ї–µ –ґ–µ–ї–µ–Ј–∞: —Н–ї–µ–Ї—В—А–Њ–љ–Њ–≤ —Б—В–∞–љ–Њ–≤–Є—В—Б—П –Љ–µ–љ—М—И–µ, —З–µ–Љ –Є–Њ–љ–Њ–≤. –Я–Њ—Б–ї–µ –≤—Л—Б—Л—Е–∞–љ–Є—П –Ї–∞–њ–ї–Є –≤–Њ–і—Л –љ–∞ –Є–Ј–Љ–µ–љ—С–љ–љ–Њ–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –њ–ї–∞—Б—В–Є–љ—Л –Њ—Б—В–∞—С—В—Б—П —А–ґ–∞–≤—З–Є–љ–∞ вАУ –Ї–Њ—А—А–Њ–Ј–Є–Њ–љ–љ–∞—П –Ї–Њ—А–Ї–∞.
–Э–∞ –Є—Б–њ—Л—В—Г–µ–Љ–Њ–є –њ–ї–∞—Б—В–Є–љ–µ, –њ–Њ–і–Ї–ї—О—З–µ–љ–љ–Њ–є –Ї —Н–Љ–Є—В—В–µ—А—Г —Н–ї–µ–Ї—В—А–Њ–љ–Њ–≤ –Ї–Њ—А—А–Њ–Ј–Є—П –љ–µ –≤–Њ–Ј–љ–Є–Ї–∞–µ—В, –≤—Б—П –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В—М –ґ–µ–ї–µ–Ј–∞ —Н–Ї–≤–Є–њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ–∞, –љ–µ—В –∞–љ–Њ–і–љ—Л—Е —Г—З–∞—Б—В–Ї–Њ–≤ –љ–∞ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є [–Ы2 —Б—В—А. 651]. –≠–Љ–Є—Б—Б–Є—П —Н–ї–µ–Ї—В—А–Њ–љ–Њ–≤ –≤ –ґ–µ–ї–µ–Ј–Њ –Є–Ј –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ–≥–Њ —Г—Б—В—А–Њ–є—Б—В–≤–∞ вАУ —Н–Љ–Є—В—В–µ—А–∞ —Н–ї–µ–Ї—В—А–Њ–љ–Њ–≤ –њ–Њ–і–і–µ—А–ґ–Є–≤–∞–µ—В —Н–ї–µ–Ї—В—А–Њ–љ–љ–Њ вАУ –Є–Њ–љ–љ—Л–є –±–∞–ї–∞–љ—Б –≤ –Ї—А–Є—Б—В–∞–ї–ї–Є—З–µ—Б–Ї–Њ–є —А–µ—И—С—В–Ї–µ –ґ–µ–ї–µ–Ј–∞ (—Н–ї–µ–Ї—В—А–Њ–љ–Њ–≤ —Б—В–∞–љ–Њ–≤–Є—В—Б—П –љ–µ –Љ–µ–љ—М—И–µ, —З–µ–Љ –Є–Њ–љ–Њ–≤) –Є —Н–Ї–≤–Є–њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ–Њ—Б—В—М –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –ґ–µ–ї–µ–Ј–∞. –Ш–Ј —Н–Љ–Є—В—В–µ—А–∞ —Н–ї–µ–Ї—В—А–Њ–љ—Л –њ–µ—А–µ—Е–Њ–і—П—В –≤ –ґ–µ–ї–µ–Ј–љ—Г—О –њ–ї–∞—Б—В–Є–љ—Г, –і–µ–є—Б—В–≤–Є–µ–Љ –Ї—Г–ї–Њ–љ–Њ–≤—Б–Ї–Є—Е —Б–Є–ї —А–∞—Б–њ—А–µ–і–µ–ї—П—О—В—Б—П –њ–Њ –µ—С –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є, –±–ї–Њ–Ї–Є—А—Г—П –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ –∞–љ–Њ–і–љ—Л—Е —Г—З–∞—Б—В–Ї–Њ–≤. –†–∞–±–Њ—В–∞—О—Й–Є–є —Н–Љ–Є—В—В–µ—А —Н–ї–µ–Ї—В—А–Њ–љ–Њ–≤ –≤ –ґ–µ–ї–µ–Ј–Њ –њ–Њ–њ–Њ–ї–љ—П–µ—В —Н–ї–µ–Ї—В—А–Њ–љ—Л –≤ –Ї—А–Є—Б—В–∞–ї–ї–Є—З–µ—Б–Ї–Њ–є —А–µ—И—С—В–Ї–µ –њ—А–Є –Є—Е –≤—Л—Е–Њ–і–µ –≤ –Ї–∞–њ–ї—О –≤–Њ–і—Л –≤ –њ–µ—А–Є–Њ–і –µ—С –≤—Л—Б—Л—Е–∞–љ–Є—П, —В–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ –њ—А–Њ–ї–Њ–љ–≥–Є—А—Г–µ—В —Д–∞–Ј—Г –≥–Є–і—А–Њ–Ї—Б–Є–і–∞ –ґ–µ–ї–µ–Ј–∞ –і–Њ –њ–Њ–ї–љ–Њ–≥–Њ –≤—Л—Б—Л—Е–∞–љ–Є—П –Є–Ј–Њ–ї–Є—А–Њ–≤–∞–љ–љ–Њ–є –Ї–∞–њ–ї–Є —Б –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –ґ–µ–ї–µ–Ј–∞:
![]()
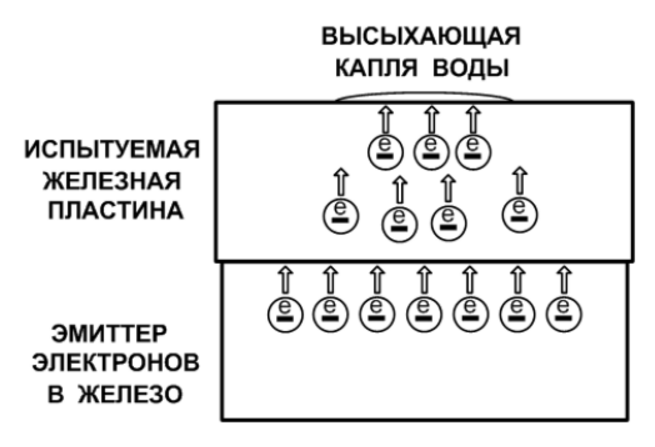
–Я—А–Є —Н—В–Њ–Љ —Д–∞–Ј–∞ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П —А–ґ–∞–≤—З–Є–љ—Л Fe2O3 –љ–µ —Г—Б–њ–µ–≤–∞–µ—В –љ–∞—Б—В—Г–њ–Є—В—М, –±–ї–Њ–Ї–Є—А—Г–µ—В—Б—П. –Я–Њ—Б–ї–µ –≤—Л—Б—Л—Е–∞–љ–Є—П –Ї–∞–њ–ї–Є –≤–Њ–і—Л –љ–∞ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –Є—Б–њ—Л—В—Г–µ–Љ–Њ–є –њ–ї–∞—Б—В–Є–љ—Л –Њ—Б—В–∞—С—В—Б—П –њ—П—В–љ–Њ —Б–µ—А–Њ–≥–Њ —Ж–≤–µ—В–∞, –µ–≥–Њ –Љ–Њ–ґ–љ–Њ —Г–і–∞–ї–Є—В—М –Љ—П–≥–Ї–Њ–є —В–Ї–∞–љ—М—О. –Я–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ–∞—П —Б—В—А—Г–Ї—В—Г—А–∞ –Є—Б–њ—Л—В—Г–µ–Љ–Њ–є –њ–ї–∞—Б—В–Є–љ—Л –љ–µ –Є–Ј–Љ–µ–љ–µ–љ–∞.
–Я–Њ —Е–Є–Љ–Є—З–µ—Б–Ї–Є–Љ —А–µ–∞–Ї—Ж–Є—П–Љ –≤ –Ї–∞–њ–ї–µ –≤–Њ–і—Л –љ–∞ –Є—Б–њ—Л—В—Г–µ–Љ–Њ–є –њ–ї–∞—Б—В–Є–љ–µ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –≤–∞—А–Є–∞–љ—В –Ї–∞—В–Њ–і–љ–Њ–є –Ј–∞—Й–Є—В—Л [–Ы1], —В–Њ–ї—М–Ї–Њ —Н–Љ–Є—Б—Б–Є–Њ–љ–љ—Л–є –Ї–∞—В–Њ–і —А–∞–±–Њ—В–∞–µ—В –±–µ–Ј –∞–љ–Њ–і–∞ вАУ –њ—А–Њ—В–µ–Ї—В–Њ—А–∞ –Ї–∞–Ї –ґ–µ–ї–µ–Ј–љ—Л–є —Б—В–Њ–ї–± –Љ–Є–љ–∞—А–µ—В–∞ –Ъ—Г—В—Г–± вАУ –Ь–Є–љ–∞—А.
21 –і–µ–Ї–∞–±—А—П 2015 –≥–Њ–і–∞.
–Ы–Є—В–µ—А–∞—В—Г—А–∞:
1. –†–µ–≤–∞—И–Є–љ –С. –У. —Б—В–∞—В—М—П ¬Ђ–ѓ–≤–ї–µ–љ–Є–µ —Г—Б—В–Њ–є—З–Є–≤–Њ–є —Н–ї–µ–Ї—В—А–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Њ–є –Ј–∞—Й–Є—В—Л –Љ–µ—В–∞–ї–ї–Њ–≤ –Њ—В –Ї–Њ—А—А–Њ–Ј–Є–Є¬ї, –Х–≤—А–∞–Ј–Є–є—Б–Ї–Є–є –љ–∞—Г—З–љ—Л–є –ґ—Г—А–љ–∞–ї вДЦ 9, —Б–µ–љ—В—П–±—А—М 2015–≥., –∞–і—А–µ—Б –≤ —Б–µ—В–Є –Є–љ—В–µ—А–љ–µ—В: www.journalPro.ru
2. –У—Г—А–Њ–≤ –Р. –Р., –С–∞–і–∞–µ–≤ –§. –Ч., –Ю–≤—З–∞—А–µ–љ–Ї–Њ –Ы. –Я., –®–∞–њ–Њ–≤–∞–ї –Т. –Э., –•–Є–Љ–Є—П. –£—З–µ–±–љ–Є–Ї –і–ї—П –≤—Г–Ј–Њ–≤. –Ь., –Є–Ј–і. –Ь–Т–Ґ–£ –Є–Љ. –Э.–≠. –С–∞—Г–Љ–∞–љ–∞, 2008. 784 —Б.
3. –Ц—Г–Ї–Њ–≤ –Р. –Я., –Ь–∞–ї–∞—Е–Њ–≤ –Р. –Ш., –Ю—Б–љ–Њ–≤—Л –Љ–µ—В–∞–ї–ї–Њ–≤–µ–і–µ–љ–Є—П –Є —В–µ–Њ—А–Є–Є –Ї–Њ—А—А–Њ–Ј–Є–Є. –Ь., –Т—Л—Б—И–∞—П —И–Ї–Њ–ї–∞, 1991. 168 —Б.









